신의료기술 의료기기 선진입 확대 ⇨ ‘바이오헬스 산업 활성화, 신의료기술 발전 촉진’
화학물질 관리제도 합리화 ⇨ ‘연구개발 활성화, 대기환경 개선, 업계부담 완화’ 등
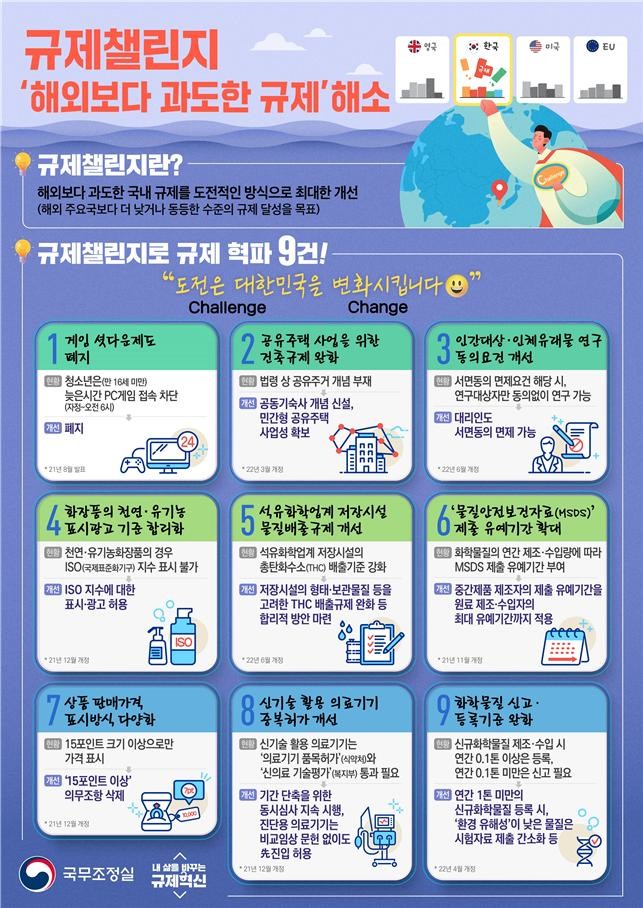
규제챌린지는 해외 주요국보다 더 낮거나 동등한 수준의 규제 달성을 목표로 한다는 점에서 ‘챌린지(Challenge)’로 명명한 것으로서 민간이 제안한 해외 주요국보다 과도한 규제를 민간.정부가 함께 집중 검토하여 최대한 개선하는 새로운 규제혁신 플랫폼이다.
지난해말 대한상공회의소는 기업에 부담이 되는 소위 갈라파고스 규제 개선을 위한 민관협력을 국무조정실에 건의하였고, 이에, 중소기업중앙회, 중견기업연합회, 벤처협회 등 경제단체를 포함하여 주한유럽상공회의소, 외국인투자 옴부즈만(KOTRA) 등 외국인 투자 관련 단체, 산업융합촉진 옴부즈만(KITECH) 등 지원기관, 한국행정연구원 등이 함께 규제챌린지를 추진했다.
특히, 경제단체는 회원사를 대상으로 ‘해외보다 규제수준이 높다고 인식’하는 규제를 직접 조사하였고, 국무조정실은 경제단체와 협의하여 해외 규제수준과 산업·국민편익 파급효과 등을 고려, 15개의 과제를 규제챌린지 과제로 선정했다.
정부는 규제챌린지가 본격적으로 시작된 금년도 6월부터 부처별 규제입증위원회와 국무조정실 주관 관계부처 협의 등을 통해 건의된 15개 과제에 대해 최종 검토 결과를 도출했다.
이중, 신기술 활용 의료기기 중복허가 개선, 화학물질 신고·등록기준 완화 등 2개 과제는 일부 개선하여 업계의 부담을 최대한 줄이기 위해 노력했다.
신기술 활용 의료기기 중복허가 개선(벤처협/복지부·식약처)에 대해서는 현재 인공지능 등 신기술을 활용한 의료기기는 식약처의 의료기기 제조 허가·인증을 위해 장비의 규격 등에 대한 심사 ‘의료기기 품목허가’ 와 복지부의 건강보험 등재 등을 위해 의료행위의 안전성과 유효성에 대한 ‘신의료 기술평가’ 대상이었다.
관련 업계는 신의료기술 활성화를 위해 관련 심사·평가기간 단축 및 임상문헌 미제출 등 규제 완화 지속 요구해왔다.
이에 따라 평가기간 단축을 위한 동시(통합)심사를 지속 추진하고, 신의료 기술에 대한 임상문헌 제출 예외 적용, 유예기간 확대 등 유예대상에 체외진단의료기기 포함해 ▴진단용 의료기기는 평가실시 이력 (탈락)에도 불구하고 1차례 시장진입을 허용하는 것으로 개선된다.
이는 신의료기술 활용 의료기기의 선진입을 통해 바이오헬스 산업 활성화, 신의료기술 발전 촉진 기여될것으로 기대된다.
화학물질 신고ㆍ등록기준 완화 (중기중앙회/환경부)에 대해서도 현재 신규화학물질 제조·수입시 연간 0.1톤 이상은 등록, 0.1톤 미만은 신고하도록 의무 부여했던 것에 대해 연간 제조·수입량 1톤으로 등록기준 상향 조정, R&D 목적 화학물질 수입요건 완화 등 화학업계가 지속 요청해왔다.
앞으로는 연간 1톤 미만의 신규화학물질 등록시 ‘환경 유해성’ 우려가 낮은 물질은 시험자료 제출 간소화(2종 면제), R&D 목적의 경우 연간 0.1톤 이하 수입시 상세 성분정보자료 제출 면제(단, 물질안전보건자료 첨부)된다.
이는 연간 1톤 미만 신규화학물질 등록시 시험자료 생산 비용·소요기간 부담 감소, R&D 화학물질 수입요건 완화으로 연구개발 활성화에 기여할것으로 기대된다.
[ⓒ 더 스타트. 무단전재-재배포 금지]